对氮化物的研究主要源于Li3N的高离子电导率(10-2S/cm),即锂离子易于迁移。然而,Li3N的分解电压相对较低(0.44V),因此不适合直接用作电极材料。锂金属氮化物的高离子导电性和过渡金属的可变化合价使其成为一种新型的锂离子电池负极材料成为可能。锂金属氮化物根据其结构可分为反萤石型和Li3N型。
属于反萤石结构的锂氮化合物包括Li7MnN4和Li3FeN2。萤石通常被称为CaF2,其结构如图1所示。氟位于面心立方位置,钙位于以氟为顶点的四面体的中心。在元素周期表中,Ti到Fe可以形成通式为Li2n-1Mn的化合物。其中,Li5TN3、Li7VN4、Li5Cr2N9、Li7MnN4、Li3FeN2等可以稳定存在。这些氮化物对应于CaF2结构,其相当于钙位点处的氮。氟的位置由锂和金属离子组成,阴离子和阳离子的排列与CaF2的排列正好相反,因此被称为反萤石结构。上述氮化物中的Ti、V和Cr已经达到最高氧化态。当Li被释放时,价态不能改变以保持系统中的电中性。因此,可以仅使用Li7MnN4和Li3FeN2作为电极材料。
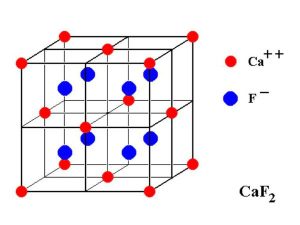
Li7MnN4和Li3FeN2可以由Li3N与金属(Mn,Fe)或金属氮化物(Mn4N,Fe4N)按一定比例,在氮气气氛中,在600~700℃下加热8-12h得到。合成反应式如下:
(3/7)Li3N+Mn+(5/6)N2=Li7MnN4
Li3N+Fe+(1/2)N2=Li3FeN2
在Li7MnN4结构中,MnN4以四面体的形式独立存在,并且锂占据点形成三维网络。锰的价态为+5,其最高价态为+7,因此锂离子的理论最大脱嵌量为2。Li7MnN4的充放电平台约为1.2V,首次脱锂至1.7V时的容量为260mA·h/g,相当于1.55的脱锂量。此时,锰呈现+6和+7两种价态。随后,在0.8~1.7V的电压范围内,可逆锂提取容量约为300mA·h/g,具有良好的循环性能。Li7MnN4在充电过程中具有第二相,放电后可以恢复到原始相,表明该材料具有良好的锂脱嵌可逆性。与Li7MnN4不同,Li3FeN2中的FeN4四面体共边缘,沿c轴形成一维链结构。从结构的角度来看,它比Li7MnN4具有更好的电子导电性。铁的价态是+3,在脱锂过程中可以变为+4。锂离子的理论最大脱嵌量为1。当脱锂量大于1时,Li3FeN2分解,分解电压约为1.5V。Li3FeN1充电。放电平台非常平坦(约1.2V),可逆锂提取容量约为150mA·h/g,在充电和放电过程中产生四个不同的相。
Li3N具有P6对称性,其结构由交替排列的Li2+N3层(A层)和Li+层(B层)组成。锂金属氮化物Li3-xMxN(M=Co,Ni,Cu)和Li3N的结构,其中Co、Ni、Cu部分取代了B层中的锂(图2以Li2.5Co0.5N为例),Li3-xMxMxN通常是以金属粉末和Li3N粉末为反应物,在氮气氛下通过高温固相法制备的。用该方法合成的Li3-xMxN固溶体的组成范围为:0≤x≤0.5(Co);0≤x≤0.6(Ni);0≤x≤0.4(Cu)。由于M2+(特别是Co2+、Ni2+)和M+共存于Li3-xMxN系统中,并形成相同数量级的锂缺陷,因此这种氮化物的准确表达式应为Li3-x-y(M+x-yM2+y)N,其中y表示锂空位。
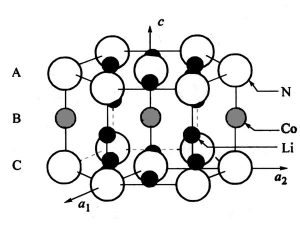
在氮化物中,Li2.6Co0.4N材料的电化学性能最好。Li2.6Co0.4N材料的平均充放电电压为0.6V,在0~1.4V电压范围内的可逆锂提取容量为760~900mA·h/g,是类石墨碳材料理论容量的两倍多。密度与石墨相当。当Li2.6Co0.4N材料首次脱锂时,相当于去除了约1.6个锂,结构式变为Li1.0Co0.4N,这意味着B层中的所有锂和A层中的一半锂被分离。当脱锂的上限电压超过1.4V时,A层可能会因脱锂过多而分解,结构会被破坏,从而导致材料失去电化学活性。在第一次脱锂过程中,材料从结晶形式变为无定形形式,并且发生一些元素的重排,并且在随后的循环中保持无定形形式。这种非晶形式可以使大量的锂离子脱嵌,这是Li2.6Co0.4N具有高脱嵌容量的主要原因。
锂离子是材料充放电过程中唯一可以脱嵌的离子,结构中的钴离子或电解质成分的阴离子不参与其中。显然,Li2.6Co0.4N中的钴为+1价,锂和氮的价态分别为+1价和-3价。对于脱锂产物Li1.0Co0.4N,每种元素的价态都更复杂。脱锂引起的稳定电荷由钴的化合价的变化来补偿,钴的化合价将从+1变为+5。钴不具有+5的高价态,因此氮的部分价态很可能在脱锂过程中也发生了变化。这意味着,当材料从锂中释放时,钴和氮在保持电荷稳定方面发挥着积极作用。认为Li2.6Co0.4N在钴和氮之间具有强共价特性,并且它不是具有强离子特性的化合物。也就是说,Li2.6Co0.4N中的氮并不都是三价的,钴的价态很难确定,它可能在+2和+3之间。有人首次研究了锂脱嵌时Li2.6Co0.4N的结构变化。结果表明,当材料首次脱硅至1.4V时,其结构发生了明显变化。A层中的氮原子偏离了原来的位置,材料发生了变化。它是无定形的。然后,在材料的下一个锂插入过程中,大部分锂被重新插入A层,并且这种脱嵌过程从短程顺序是可逆的。
Li3-xCuxN和Li3-xNixN材料在可逆脱嵌容量和其他性能方面远不如Li2.6Co0.4N材料,因此研究较少。Li2.6Co0.4N材料在0~1.3V的电压范围内具有650mA·h/g的锂插入和脱附容量,其循环性能相对稳定。Li2.5Co0.5N材料的性能较差,在0~1.4V的电压范围内,锂的插入和去除能力小于250mA·h/g。尽管这三种材料也具有类似Li3N的结构,但它们的微观结构可能存在差异。例如,材料脱锂后形成的非晶态与锂周围的电子环境不同,这导致锂脱嵌的机制不同,从而表现出完全不同的电化学性质。
与其他负极材料不同,Li3-xMxN(M=Co,Ni,Cu)具有富锂结构,其充电和放电电压比类石墨碳材料高几百毫伏。因此,作为负极材料,需要贫锂的5V正极。材料与之相对应;或者它可以在预先去除部分锂之后与富含锂的LiCoO2和其他正极材料结合使用。利用Li2.6Co0.4N的第一次除锂能力大于第一次嵌锂能力的特点,可以与一些初始不可逆容量较高的负极材料(如SiO、SnxO等)结合形成高性能复合电极,提高初始充放电效率。
在许多锂金属氮化物材料中,通常认为只有Li3-xMxN(M=Co,Ni,Cu)具有Li3N结构。研究表明,将Li3N粉末预压制成块状,放入装有300kPa氮气的纯铁容器中,在850至1050°C的温度下加热12h,然后进行淬火处理,获得Li2.7Fe0.3N材料。通过该方法制备的Li2.7Fe0.3N也具有类似Li3N的结构,在0.0~1.3V的电压范围内,可逆锂提取容量为550mA·h/g。与Li2.6Co0.4N不同,Li2.7Fe0.3的第一脱锂曲线具有两个电压平台,这可能与该结构的a层和B层中的锂有关。此外,该材料在第一次脱锂后也转化为无定形形式,具体脱嵌机理有待进一步研究。